Информация о происхождении каждого из атомов в молекуле пуринового основания получена в процессе радиоизотопных исследований.
На слайде-плёнке №4 показано происхождение атомов азота и углерода пуринового кольца.
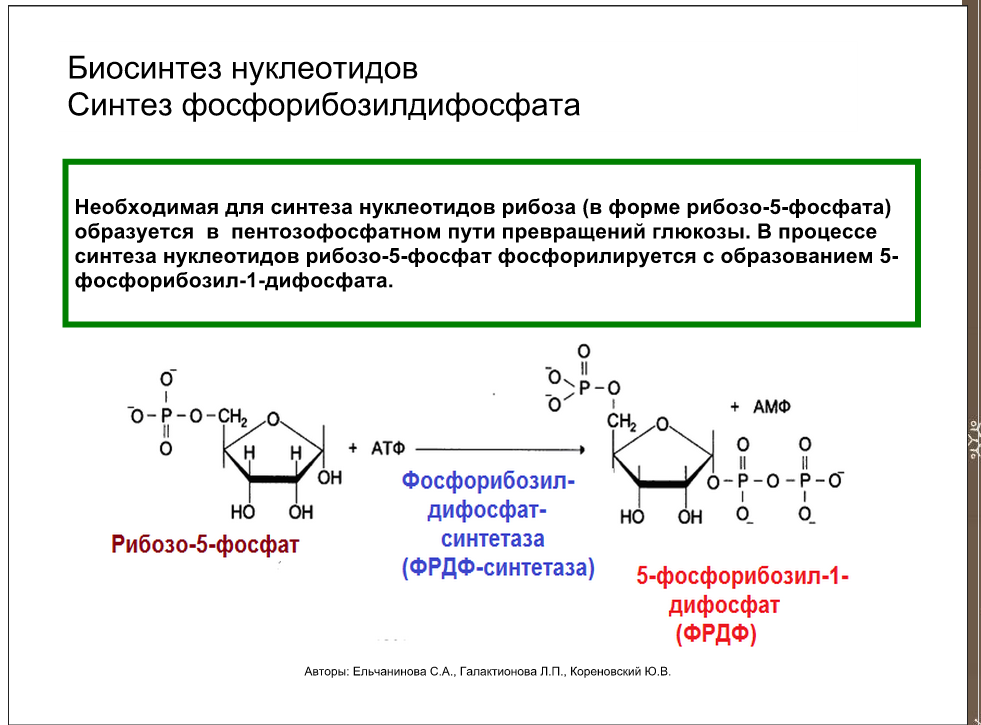
Первая стадия – образование 5-фосфорибозил-1-пирофосфата (ФРПФ) является общей как для пуриновых, так и пиримидиновых нуклеотидов.
В реакции второй стадии, катализируемой ФРПФ-амидотрансферазой, из ФРПФ и глутамина образуется глутамат и 5-фосфорибозиламин. (слайд-плёнка №5). Далее, 5-фосфорибозиламин вступает в реакцию с глицином и образуется глицил-амидориботид (ГАР). Затем амидная группа глутамина служит источником азота в будущем пуриновом кольце (№9), а глицин – в положениях углерода С-4 и С-5, а также атом азота в положении N7.
Глутамин является также донором амидной группы для атома азота N3. Путём амидировани С-4 (углеродного атома глицина). Затем атом азота N7 молекулы глицин-амидрибозилфосфитамина формируется N5, N10 – метилентетрагидрофолатом, в результате чего атом углерода займёт положение С-8. В результате замыкается имидазольное кольцо будущего пурина и лишь после этого идёт фиксирование «СО2» (карбоксибиотинэнзим), углерод которого займёт положение С-6. Атом азота (N-1) происходит из аспартата (транаминирование), а углерод С-2 образует N10-формитетрагидрофолат. Замыкание кольца катализирует фермент инозинмонофосфат-цилогидролаза.
Существенную роль играет в синтезе пуринов обмен фолиевой кислоты, в частности, кофермента тетрагидрофолата (ТГФК). Ингибирование обмена фолатов оказывает тормозящее влияние на синтезе пуринов de novo.
Образование адениловых и гуаниловых нуклеотидов происходит из инозинмонофосфата. Аденозинмонофосфат образуется через аденилосукцинат с участием аденилосукцинатсинтетазы и затем реакция катализируется аденилатсукциназой. Гуанозинмонофосфат синтезируется через ксантинмонофосфат с участием ИМФ-дегидрогеназы, а далее путём аминирования с глутамином (слайд-плёнка №6).
Имеется «запасной» путь синтеза пуриновых нуклеотидов (или путь «спасения»), когда довольно быстро накапливаются АМФ и ГМФ. Этот путь (слайд-плёнка №7) сводится к образованию АМФ и пирофосфата в реакции, где участвуют аденин и ФРПФ. Реакция катализируется аденозинфосфо-рибозилтрансферазой. Аналогично ГМФ образуется из гуанина с участием ФРПФ, а реакция катализируется гуанинфосфорибозилтрансферазой. Возможно также образование инозинмонофосфата (ИМФ) из гипоксантина и ФРПФ с участием того же фермента.
Превращение АМФ и ГМФ в соответствующие ди- и трифосфаты осуществляется в две стадии. Реакция фосфорилирования – перенос фосфатных групп от АТФ – осуществляется нуклеозидмонофосфаткиназой и нуклеозиддифосфаткиназой.
Регуляция биосинтеза пуринов. Важнейшую роль играет внутриклеточная концентрация ФРПФ. Она определяется соотношение скоростей его синтеза, утилизации и деградации (слайд-плёнка №8). На слайде показано, что ФПФ-амидотрансфераза – первый из ферментов, участвующих в процессе синтеза пуриновых нуклеотидов и ингибируется АМФ и ГМФ по принципу обратной связи.
б) Биосинтез пиримидиновых нуклеотидов.
Структура ядра пиримидинов проще и путь их биосинтеза короче, чем у пуринов. В то же время оба пути имеют ряд общих предшественников: ФРПФ, глутамин, СО2 и аспартат. Синтез пиримидинового кольца (слайд-плёнка №9) начинается с образования карбамаилфосфата из глутамина, АТФ и СО2 в реакции, катализируемой в цитозоле карбамоилфосфатсинтетазой (II), тогда как для синтеза мочевины этот фермент находится в митохондриях и обозначен как №1 (карбамоилфосфатсинтетаза 1).
Первый этап – образование карбамоиласпартата, который катализируется аспартаттранскарбамоилазой. Затем фермент дигидрооротаза выщепляет Н2О и образуется кольцевая структура.
Читайте также: Как может испортится ткань
На следующем этапе происходит действие дигидрооротатдегидрогеназы (кофермент НАД) с образованием оротовой кислоты. Далее, к оротовой кислоте присоединяется остаток рибозофосфата с образованием оротидинмонофосфата (ОМФ).
Первый пиримидиновый рибонуклеотид уридинмонофосфат (УМФ) образуется при декарбоксилировании ОМФ. Далее образование цитидинмонофосфата (ЦМФ) происходит путём аминирования УМФ, когда в реакции участвует глутамин и АТФ.
Фосфорилирование УМФ и ЦМФ до соответствия ди- и трифосфатов происходит аналогично тому, как это описано для пуриновых нуклеотидов.
Образование тимидинмонофосфата (ТМФ) требует участия производного тетрагидрофолата в качестве донора одноуглеродного фрагмента. Поэтому
остановимся, прежде всего, на синтезе пуриновых и пиримидиновых дезоксирибонуклеотидов. Вначале нуклеозидмонофосфат переходит за счёт траты энергии АТФ с участием киназы в нуклеозидфосфат. Затем (слайд-плёнка №10).
Продолжим описание синтеза тимидинмонофосфата (ТМФ). Итак, дезокси-УМФ метилируется тимидиласинтазой, использующей N5, N10-метилентетрафолат как донор метильной группы. Метиленовая группа тетрафтолата (от витамина Вс – фолиевой кислоты) восстанавливается в ходе реакции до метильной и присоединяется к атому С-5 дезокси-УМФ. Происходит одновременное окисление тетрагидрофолата до дигидрофолата. Восстановление дигидрофолата происходит с участием дигидрофтолатредуктазы.
Известно, что делящиеся клетки (злокачественный рост) активно синтезируют ТМФ с образованием дигидрофолата. Ингибитором редуктазы дигидрофолата является метотрексан (аметоптерин), который широко используется как противоопухолевый препарат.
Другим противоопухолевым препаратом является 5-фторурацил, который фосфориблизируется ферментом оротат-фосфорибозилтрансферазой и т.о. является конкурентным ингибитором, что тормозит образование ОМФ, а затем и ТМФ. Другой препарат – аллонуринол – также фосфориболизируется этим ферментом, поэтому может выступать в качестве лечебного противоопухолевого препарата.
Регуляция биосинтеза пиримидинов. Путь биосинтеза пиримидиновых нуклеотидов регулируется двумя различными механизмами, т.е. аллостерическим типом и по принципу обратной связи. Кроме того, ряд ферментов синтеза являются объектами координированной репрессии – депрессии.
Карбамоилфосфатсинтаза ингибируется УТФ, пуриновыми нуклеотидами, но активируется ЦРПФ. Другой фермент аспартаткарбамоилтрансфераза ингибируется УТФ (слайд-плёнка №11 ).
Понятие о нуклеопротеидах, их превращения в желудочно-кишечном тракте. Строение, биологическая роль, особенности обмена мононуклеотидов в организме человека.
Нуклеопротеиды – сложные белки, небелковая часть который представлена нуклеиновыми кислотами (ДНК и РНК)(белок – гистон)

Мононуклеотид – мономер нуклеиновых кислот, состоит из остатка фосфорной кислоты, азотистого основания и пентозы. Мононуклеотиды связаны 3’,5’-диэфирными связями между рибозами соседних мононуклеотидов через остаток фосфорной кислоты.
Биологическая роль мононуклеотидов:
— субстраты для синтеза ДНК и РНК;
— Структурная. Из мононуклеотидов построены:нуклеиновые кислоты, некоторые коферменты,простетические группы ферментов
— Энергетическая. Содержат макроэргические связи — являются аккумуляторами энергии. АТФ — это универсальный аккумулятор энергии
— Сигнальная. Мононуклеотиды — аллостерические эффекторы многих ключевых ферментов. цАМФ и цГМФ являются посредниками в передаче гормонального сигнала.
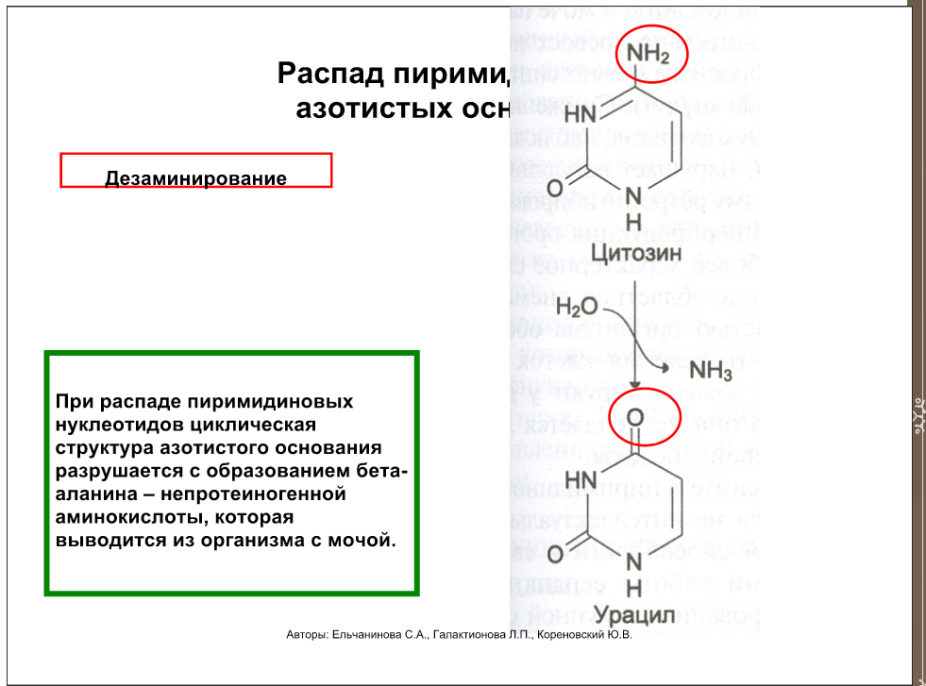
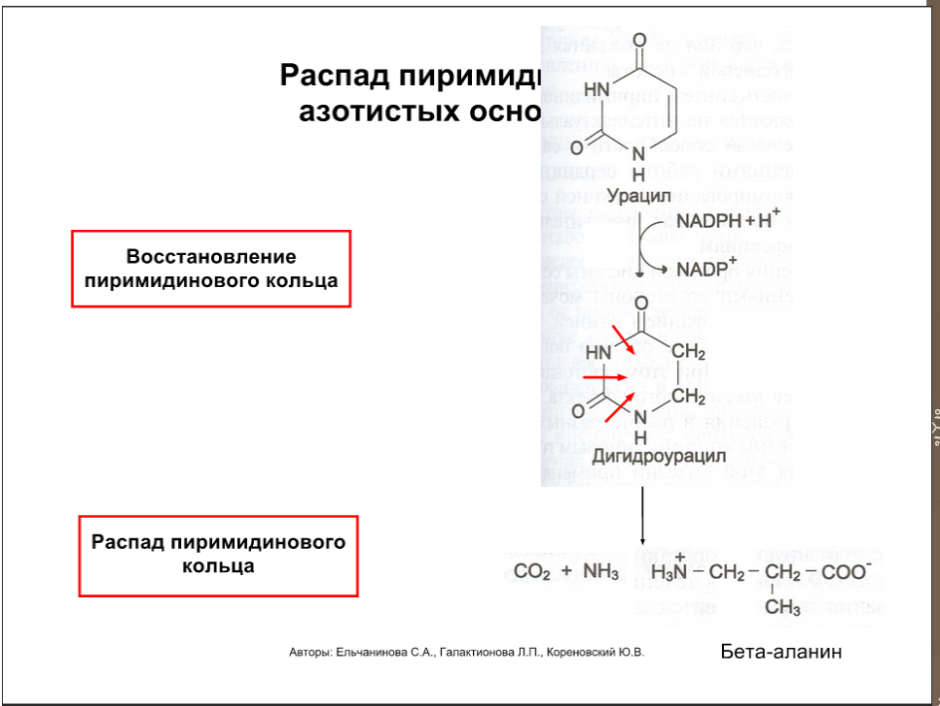
Особенности – из мононуклеотидов лишь малая часть действительно используется, остальные либо в энтероцитах же превращаются в мочевую кислоту, либо под влиянием микрофлоры расщепляются до аммиака, углекислого газа, бета-аланина и бета-аминоизобутирата.
Биосинтез пуриновых нуклеотидов. Источники атомов пуринового кольца, реакции синтеза, роль витаминов В9 и В12.
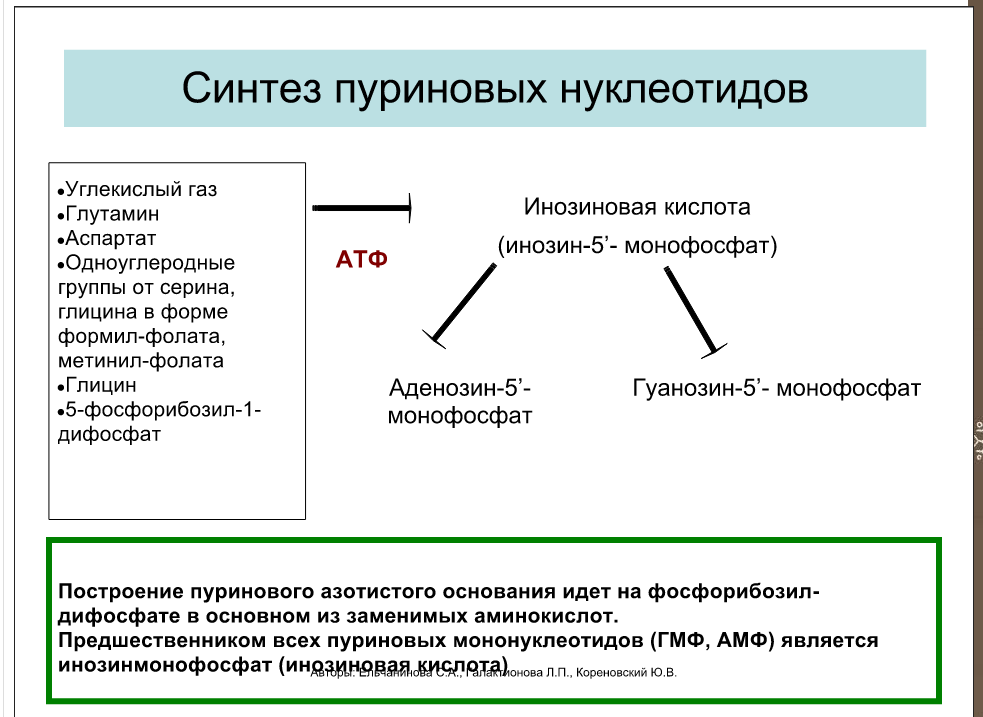
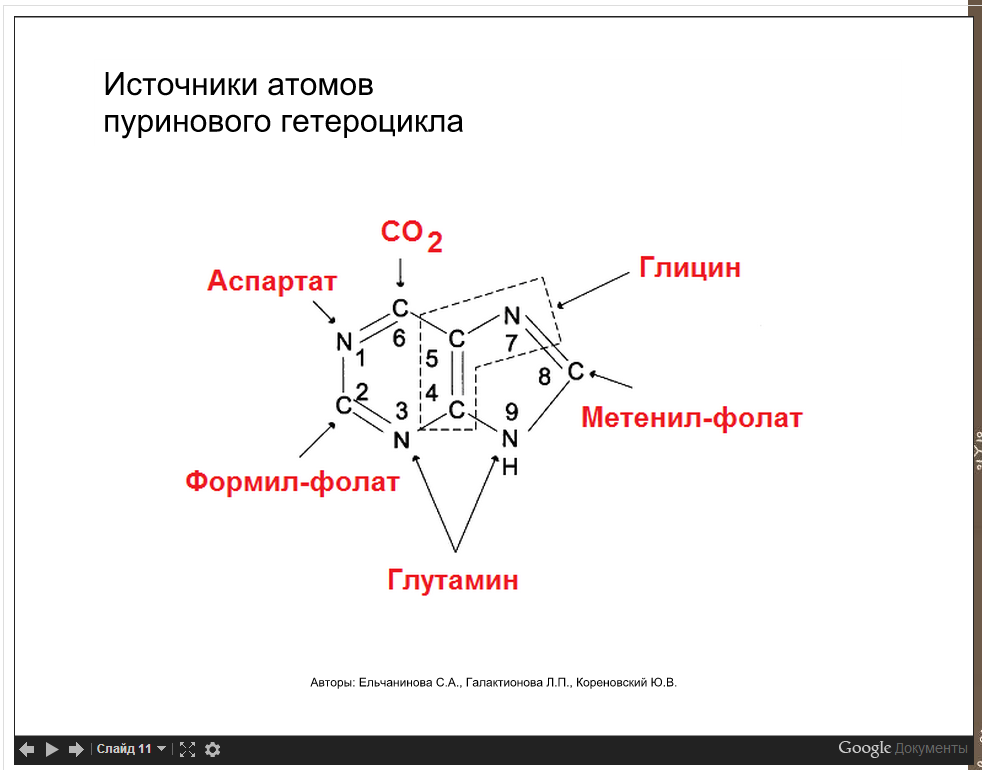
Формил фолат и метенил фолат – производные витамина B9, а витамин В12 участвует в этих превращениях витамина В9.
Читайте также: Изменение структуры костной ткани будет наблюдаться
Биосинтез пиримидиновых нуклеотидов. Источники атомов пиримидинового кольца, реакции синтеза, роль витаминов В9 и В12.

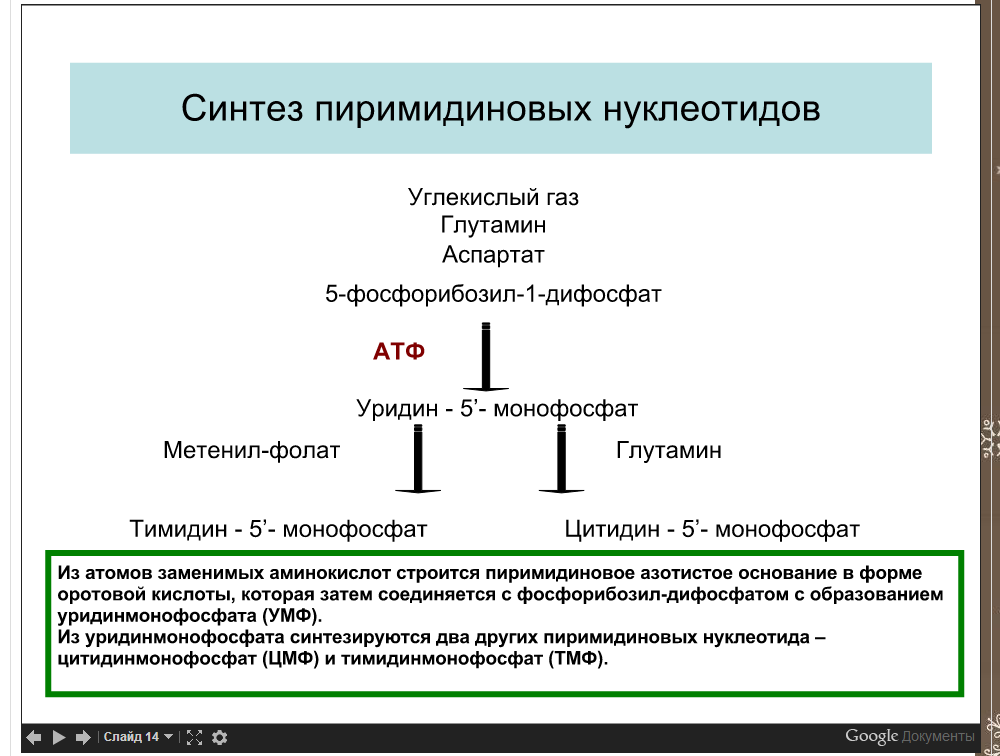
В9 служит субстратом для синтеза кофермента, необходимого для превращения УМФ в ТМФ, В12 участвует в синтезе этого кофермента.
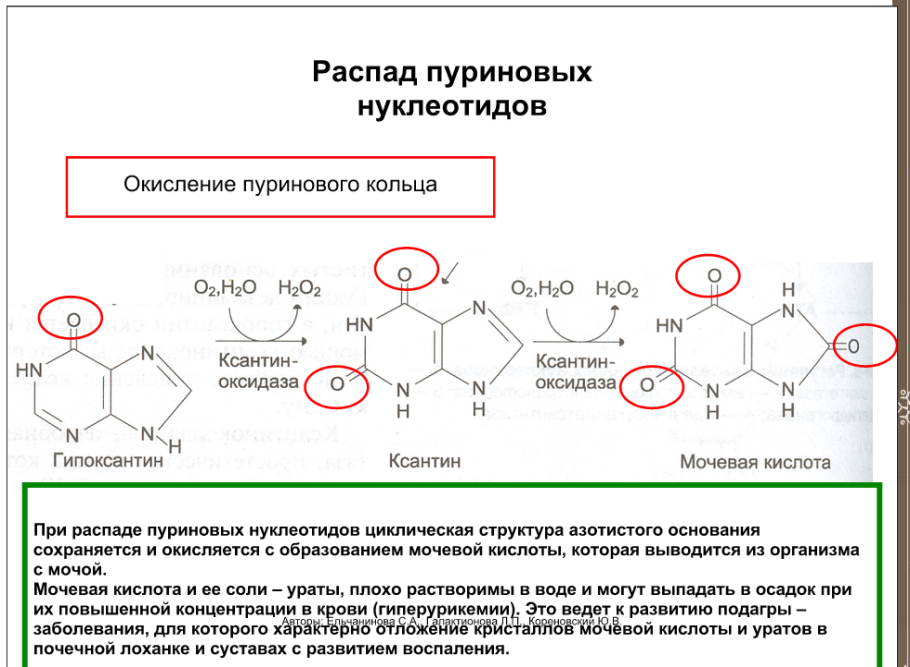
Распад пуриновых и пиримидиновых нуклеотидов. Особенности и реакции процесса распада, конечные метаболиты. Нарушения обмена пуриновых нуклеотидов при подагре.
Если пуриновых оснований образуется слишком много, то при их катаболизме образуется слишком высокое количество мочевой кислоты, что приводит к подагре.
Подагра – причина – врожденная недостаточность ферментов, осуществляющих превращение гипоксантина в инозиновую кислоту и пуриновые азотистые основания.
Способствует развитию: красное вино, сыр, кофе; белковая пища; малоподдвижный образ жизни
Лечение – конкурентный ингибитор ксантиноксидазы – АЛЛОПУРИНОЛ.
Где распад пуринов, то там гипоксантин образуется из аденина (под действием адениндезаминазы)
Строение ДНК и РНК. Химические связи, участвующие в формировании их структуры. Функции нуклеиновых кислот. Виды переноса генетической информации. Биологическая роль комплементарности азотистых оснований.
ДНК и РНК – полимеры, мономерами которых являются мононуклеотиды. (ДНК в качестве пентозы имеет дезоксирибозу, а РНК – рибозу). ДНК имеет первичную (цепь дезоксирибонуклеозидмонофосфатов соединённых 3’ 5’ фосфодиэфирной связью), вторичную (две таких цепочки соединённых с помощью водородных связей между азотистыми основаниями. Между А и Т две связи, Г и Ц – три), третичную (ДНК упакованная в виде хромосомы) структуру.
РНК. Первичная – рибонуклеозидмонофосфаты в одну цепочку с 3 5 фосфодиэфирными связями. Вторичная – одноцепочечная цепь, в которой между азотистыми основаниями образуются водородные связи. Причём не все основания буду компелментарны, так что будут образовываться несвязанные участки, которые будут как бы выпирать из цепочки. Третичная – структура, в которой образуются ещё дополнительные связи между или нуклеотидными остатками, удалёнными друг от друга, либо между основаниями и остатками рибозы. Такая структура стабилизирована ионами двухвалентных металлов.
ДНК – хранение наследственной информации. РНК – мРНК – служит матрицей для синтеза белка (реализация наследственной инфы), тРНК – транспорт своей аминокислоты в рибосомам для синтеза белка. рРНК – участвуют в создании рибосом, а значит и непосредственно в трансляции. Репликация (удвоение ДНК), транскрипция – перенос генетической информации с ДНК на РНК, трансляция – синтез белка.
Биологическая роль комплементарности азотистых оснований – обеспечивает точный перенос генетической информации.
Репликация. Механизм и биологическое значение. Теломера и теломераза. Понятие о репликативной старости клетки.
Репликация – удвоение ДНК с помощью спец.фермента ДНК-полимеразы, происходит в ядре клетки в S фазу клеточного цикла, предшествует делению клетки. Происходит в несколько стадий.
ДНК- полимераза способна наращивать цепь ДНК только на 3΄– конце. Иницианцию репликации регулируют сигнальные белки – факторы роста.
Удвоение ДНК основано на том, что при расхождении нитей к каждой нити можно достроить комплементарную копию, таким образом, получая две молекулы ДНК, копирующие исходную.
инициация – разрушение водородных связей и расхождение нитей (образование множества репликативных вилок)
элонгация – удлинение дочерних нитей, исключение праймеров
терминация – завершение двух дочерних цепей ДНК
ДНК-полимераза не может начать процесс синтеза сама, ей нужна «затравка», в качестве такой затравки используется фрагмент РНК. А теперь подробнее…
Читайте также: Что означает обызвествление в мягких тканях
Инициация: 1) начинается с расплетения участка ДНК – образуется репликативная вилка ( с участием геликазы).2) у 3΄–го конца закрепляется РНК-затравка(праймер) , на другой нити закрепляются несколько праймеров.
Элонгация: 1) синтез дочерних нитей ДНК начинается с участка РНК-праймера. 2) Полимеризация мононуклеотидов, которые выстраиваются вдоль матрицы по принципу комплементарности с участием ДНК-полимераз (активируются РНК-праймеры) 3) считывание информации идет с 3-го конца к 5-му концу (строится цепь 5-3 лидирующая. 4) на другой нити – полимеризация дезоксирибонуклеотидов: строятся ферменты. Оказаки – отстающая.
Терминация: 1) Праймеры вырезаются, и происходит сшивка фрагментов ДНК-полимеразой. 2) Образуется двойная спираль, которая сформирована дочерней и материнской нитями ДНК 3) одновременно репликация идет в нескольких местах ДНК по всем направлениям – сайты репликации.
В каждой нити ДНК на 5′- конце имеются особые участки, содержащие частые повторы (ГГГТТА)- теломеры. Их роль — стоп-сигнал при повторяющейся репликации. Эти участки ДНК не копируются и не достраиваются, поэтому каждое новое деление сопровождается укорочением теломеры.
Существует критическая длина теломеры, при которой клетка утрачивает способность к репликации (делению) – репликативная старость. Репликативное старение лежит в основе старения организма. (В среднем клетка проходит 50-60 репликаций, у долгожителей больше)
В эмбриональных клетках открыт фермент – теломераза, который способен достраивать теломеры после репликации. Если вводить в клетку теломеразу, открывается возможность продление жизни клетки. Например введение стволовых клеток – обновление тканей, предупреждение старения
Повреждения ДНК спонтанные и индуцированные. Процессы репарации ДНК и их возможные последствия. Мутации. Роль мутаций в эволюции и возникновении наследуемых заболеваний. Понятие о генной терапии.
Спонтанные – не вызванные внешними факторами (ошибка репликации, дезаминирования нуклеотидов, депуринизации), индуцированные – вызванные внешними факторами (в основном радиация и химия)
Повреждения ДНК исправляются – репарация с участием репаративных семейств ферментов, которые вырезают поврежденные участки и образуется АП-сайт, в котором достраивается ДНК с «правильными» азотистыми основаниями и нуклеотидами. При врожденной недостаточности репаративных ферментов – МУТАЦИИ.
Репаративная система включает : 1)белки-ферменты, узнающие ошибку 2) белки-ферменты, разрезающие в этом месте цепочку. 3) ДНК-полимеразы, достраивающие цепь. 3) ДНК-лигазы, сшивающие нить, завершают репарацию.
Мутации – изменение структуры ДНК, следствием которого является изменение синтезируемых белков.
Мутации – основной поставщик материала для эволюции. (произошла мутация, в результате которой у слона хобот стал длинным, что пипец как удобно, когда ты жрёшь траву с деревьев. Вот этот слоняра с длинным хоботом стал наиболее приспособленным, выжил, дал потомство и теперь все слоны с длинными хоботами).
Мутации могут быть в соматических клетках – тогда болеет сам человек, или в половых – тогда сам организм не страдает, а вот потомство получит эту самую мутацию, что и будет называться «наследственное заболевание»
Генная терапия – лечение наследственных, многофакторных и инфекционных заболеваний путём введения в соматические клетки пациентов ген, который обеспечивает исправление генных дефектов или придаёт клеткам новые функции.
- Свежие записи
- Балкон в многоквартирном доме: является ли он общедомовым имуществом?
- Штраф за остекление балкона в 2022: что это и как избежать наказания
- Штраф за мусор с балкона: сколько заплатить за выбрасывание окурков
- Оформление балконного окна: выбираем шторы из органзы
- Как выбрать идеальные шторы для маленькой кухни с балконом
